Scandiwm, gyda symbol elfen Sc a rhif atomig o 21, mae'n hawdd ei hydoddi mewn dŵr, gall ryngweithio â dŵr poeth, ac mae'n tywyllu'n hawdd yn yr awyr. Ei brif falens yw +3. Yn aml caiff ei gymysgu â gadoliniwm, erbiwm, ac elfennau eraill, gyda chynnyrch isel a chynnwys o tua 0.0005% yn y gramen. Defnyddir scandiwm yn aml i wneud gwydr arbennig ac aloion tymheredd uchel ysgafn.
Ar hyn o bryd, dim ond 2 filiwn tunnell yw'r cronfeydd profedig o sgandiwm yn y byd, ac mae 90 ~ 95% ohonynt wedi'u cynnwys mewn mwynau bocsit, ffosfforit a haearn titaniwm, a rhan fach mewn mwynau wraniwm, thoriwm, twngsten a phridd prin, wedi'u dosbarthu'n bennaf yn Rwsia, Tsieina, Tajikistan, Madagascar, Norwy a gwledydd eraill. Mae Tsieina yn gyfoethog iawn o ran adnoddau sgandiwm, gyda chronfeydd mwynau enfawr sy'n gysylltiedig â sgandiwm. Yn ôl ystadegau anghyflawn, mae cronfeydd sgandiwm yn Tsieina tua 600,000 tunnell, sydd wedi'u cynnwys mewn dyddodion bocsit a ffosfforit, dyddodion twngsten gwythiennau porffyri a chwarts yn Ne Tsieina, dyddodion pridd prin yn Ne Tsieina, dyddodiad mwyn haearn pridd prin Bayan Obo ym Mongolia Fewnol, a dyddodiad magnetit titaniwm fanadiwm Panzhihua yn Sichuan.
Oherwydd prinder scandiwm, mae pris scandiwm hefyd yn uchel iawn, ac ar ei anterth, roedd pris scandiwm wedi chwyddo i 10 gwaith pris aur. Er bod pris scandiwm wedi gostwng, mae'n dal i fod bedair gwaith pris aur!
Darganfod Hanes
Ym 1869, sylwodd Mendeleev ar fwlch mewn màs atomig rhwng calsiwm (40) a thitaniwm (48), a rhagfynegodd fod elfen màs atomig canolradd heb ei darganfod yma hefyd. Rhagfynegodd mai ei ocsid yw X ₂ O Å. Darganfuwyd scandiwm ym 1879 gan Lars Frederik Nilson o Brifysgol Uppsala yn Sweden. Fe'i tynnodd o'r mwynglawdd aur prin du, mwyn cymhleth sy'n cynnwys 8 math o ocsidau metel. Mae wedi echdynnuOcsid erbiwm(III)o fwyn aur prin du, ac a gafwydOcsid Ytterbiwm(III)o'r ocsid hwn, ac mae ocsid arall o elfen ysgafnach, y mae ei sbectrwm yn dangos ei fod yn fetel anhysbys. Dyma'r metel a ragfynegwyd gan Mendeleev, y mae ei ocsid ynSc₂O₃Cynhyrchwyd y metel scandiwm ei hun oClorid sgandiwmtrwy doddi electrolytig ym 1937.
Mendeleev
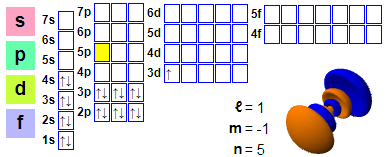
Cyfluniad electron
Ffurfweddiad electronau: 1s2 2s2 2p6 3s2 3p6 4s2 3d1
Mae scandiwm yn fetel trawsnewidiol meddal, gwyn arian gyda phwynt toddi o 1541 ℃ a phwynt berwi o 2831 ℃.
Am gyfnod sylweddol ar ôl ei ddarganfod, ni ddangoswyd y defnydd o sgandiwm oherwydd ei anhawster i'w gynhyrchu. Gyda gwelliant cynyddol mewn dulliau gwahanu elfennau daear prin, mae llif proses aeddfed bellach ar gyfer puro cyfansoddion sgandiwm. Gan fod sgandiwm yn llai alcalïaidd nag yttriwm a Lanthanid, yr hydrocsid yw'r gwannaf, felly bydd y mwynau cymysg elfen ddaear prin sy'n cynnwys sgandiwm yn cael eu gwahanu oddi wrth yr elfen ddaear prin trwy'r dull "gwaddodiad cam" pan gaiff sgandiwm(III) hydrocsid ei drin ag amonia ar ôl ei drosglwyddo i doddiant. Y dull arall yw gwahanu sgandiwm nitrad trwy ddadelfennu pegynol nitrad. Gan mai sgandiwm nitrad yw'r hawsaf i'w ddadelfennu, gellir gwahanu sgandiwm. Yn ogystal, mae adferiad cynhwysfawr y sgandiwm cysylltiedig o wraniwm, thoriwm, twngsten, tun a dyddodion mwynau eraill hefyd yn ffynhonnell bwysig o sgandiwm.
Ar ôl cael cyfansoddyn scandiwm pur, caiff ei drawsnewid yn ScCl Å a'i gyd-doddi â KCl a LiCl. Defnyddir y sinc tawdd fel y catod ar gyfer electrolysis, gan achosi i scandiwm waddodi ar yr electrod sinc. Yna, caiff y sinc ei anweddu i gael scandiwm metelaidd. Mae hwn yn fetel gwyn arian ysgafn gyda phriodweddau cemegol gweithredol iawn, a all adweithio â dŵr poeth i gynhyrchu nwy hydrogen. Felly mae'r scandiwm metel a welwch yn y llun wedi'i selio mewn potel a'i amddiffyn â nwy argon, fel arall bydd scandiwm yn ffurfio haen ocsid melyn tywyll neu lwyd yn gyflym, gan golli ei lewyrch metelaidd sgleiniog.
Cymwysiadau
Diwydiant goleuo
Mae defnyddiau scandiwm wedi'u crynhoi mewn cyfeiriadau llachar iawn, ac nid yw'n or-ddweud ei alw'n Fab y Goleuni. Gelwir yr arf hud cyntaf o scandiwm yn lamp sodiwm scandiwm, y gellir ei ddefnyddio i ddod â golau i filoedd o gartrefi. Mae hwn yn halid metel Golau trydan: mae'r bwlb wedi'i lenwi â sodiwm ïodid a scandiwm triïodid, ac ychwanegir ffoil scandiwm a sodiwm ar yr un pryd. Yn ystod rhyddhau foltedd uchel, mae ïonau scandiwm ac ïonau sodiwm yn allyrru golau o'u tonfeddi allyriadau nodweddiadol yn y drefn honno. Llinellau sbectrol sodiwm yw 589.0 a 589.6 nm, dau olau melyn enwog, tra bod llinellau sbectrol scandiwm yn 361.3 ~ 424.7 nm, cyfres o allyriadau golau uwchfioled a glas agos. Gan eu bod yn ategu ei gilydd, y lliw golau cyffredinol a gynhyrchir yw golau gwyn. Oherwydd bod gan lampau sodiwm scandiwm nodweddion effeithlonrwydd goleuol uchel, lliw golau da, arbed pŵer, oes gwasanaeth hir, a gallu torri niwl cryf y gellir eu defnyddio'n helaeth ar gyfer camerâu teledu, sgwariau, lleoliadau chwaraeon, a goleuadau ffyrdd, ac fe'u gelwir yn ffynonellau golau trydydd cenhedlaeth. Yn Tsieina, mae'r math hwn o lamp yn cael ei hyrwyddo'n raddol fel technoleg newydd, tra mewn rhai gwledydd datblygedig, defnyddiwyd y math hwn o lamp yn helaeth mor gynnar â dechrau'r 1980au.
Yr ail arf hudolus sydd gan sgandiwm yw celloedd ffotofoltäig solar, a all gasglu'r golau sydd wedi'i wasgaru ar y ddaear a'i droi'n drydan i yrru cymdeithas ddynol. Sgandiwm yw'r metel rhwystr gorau mewn celloedd solar silicon lled-ddargludyddion inswleiddio metel a chelloedd solar.
Gelwir ei drydydd arf hud yn ffynhonnell pelydr γA, gall yr arf hud hwn ddisgleirio'n llachar ar ei ben ei hun, ond ni all y llygad noeth dderbyn y math hwn o olau, mae'n llif ffoton egni uchel. Fel arfer, rydym yn echdynnu 45Sc o fwynau, sef yr unig isotopau Naturiol o sgandiwm. Mae pob niwclews 45Sc yn cynnwys 21 proton a 24 niwtron. Gellir defnyddio 46Sc, isotop ymbelydrol artiffisial, fel ffynonellau ymbelydredd γ neu gellir defnyddio atomau olrhain hefyd ar gyfer radiotherapi tiwmorau malaen. Mae yna gymwysiadau hefyd fel laser garnet yttriwm, galliwm, sgandiwm,Fflworid scandiwmFfibr optegol is-goch gwydr, a thiwb pelydr catod wedi'i orchuddio â sgandiwm ar y teledu. Ymddengys bod sgandiwm yn cael ei eni â disgleirdeb.
Diwydiant aloi
Mae sgandiwm yn ei ffurf elfennol wedi cael ei ddefnyddio'n helaeth ar gyfer dopio aloion alwminiwm. Cyn belled ag y bydd ychydig filfedau o sgandiwm yn cael ei ychwanegu at alwminiwm, bydd cyfnod Al3Sc newydd yn cael ei ffurfio, a fydd yn chwarae rhan Metamorffedd mewn aloi alwminiwm ac yn gwneud i strwythur a phriodweddau'r aloi newid yn sylweddol. Gall ychwanegu 0.2% ~ 0.4% Sc (sy'n debyg iawn i gyfran ychwanegu halen at lysiau wedi'u ffrio gartref, dim ond ychydig bach sydd ei angen) gynyddu tymheredd ailgrisialu'r aloi 150-200 ℃, a gwella cryfder tymheredd uchel, sefydlogrwydd strwythurol, perfformiad weldio, a gwrthsefyll cyrydiad yn sylweddol. Gall hefyd osgoi'r ffenomenon brau sy'n hawdd digwydd yn ystod gwaith hirdymor ar dymheredd uchel. Mae gan aloi alwminiwm cryfder uchel a chaledwch uchel, aloi alwminiwm weldiadwy newydd sy'n gwrthsefyll cyrydiad cryfder uchel, aloi alwminiwm tymheredd uchel newydd, aloi alwminiwm sy'n gwrthsefyll arbelydru niwtron cryfder uchel, ac ati, ragolygon datblygu deniadol iawn mewn awyrofod, awyrenneg, llongau, adweithyddion niwclear, cerbydau ysgafn a threnau cyflym.
Mae scandiwm hefyd yn addasydd rhagorol ar gyfer haearn, a gall ychydig bach o scandiwm wella cryfder a chaledwch haearn bwrw yn sylweddol. Yn ogystal, gellir defnyddio scandiwm hefyd fel ychwanegyn ar gyfer aloion twngsten a chromiwm tymheredd uchel. Wrth gwrs, yn ogystal â gwneud dillad priodas i eraill, mae gan scandiwm bwynt toddi uchel ac mae ei ddwysedd yn debyg i alwminiwm, ac fe'i defnyddir hefyd mewn aloion ysgafn pwynt toddi uchel fel aloi titaniwm scandiwm ac aloi magnesiwm scandiwm. Fodd bynnag, oherwydd ei bris uchel, dim ond mewn diwydiannau gweithgynhyrchu pen uchel fel gwennol ofod a rocedi y caiff ei ddefnyddio'n gyffredinol.
Deunydd ceramig
Defnyddir scandiwm, sylwedd sengl, yn gyffredinol mewn aloion, ac mae ei ocsidau'n chwarae rhan bwysig mewn deunyddiau ceramig mewn ffordd debyg. Mae gan y deunydd ceramig zirconiwm tetragonal, y gellir ei ddefnyddio fel deunydd electrod ar gyfer celloedd tanwydd ocsid solet, briodwedd unigryw lle mae dargludedd yr electrolyt hwn yn cynyddu gyda thymheredd cynyddol a chrynodiad ocsigen yn yr amgylchedd. Fodd bynnag, ni all strwythur crisial y deunydd ceramig hwn ei hun fodoli'n sefydlog ac nid oes ganddo werth diwydiannol; Mae angen dopio rhai sylweddau a all drwsio'r strwythur hwn er mwyn cynnal ei briodweddau gwreiddiol. Mae ychwanegu 6 ~ 10% o ocsid scandiwm fel strwythur concrit, fel y gellir sefydlogi zirconiwm ar ddellt sgwâr.
Mae yna hefyd ddeunyddiau ceramig peirianneg fel silicon nitrid cryfder uchel a gwrthsefyll tymheredd uchel fel dwysyddion a sefydlogwyr.
Fel dwysydd,Ocsid scandiwmgall ffurfio cyfnod anhydrin Sc2Si2O7 ar ymyl gronynnau mân, gan leihau anffurfiad tymheredd uchel cerameg peirianneg. O'i gymharu ag ocsidau eraill, gall wella priodweddau mecanyddol tymheredd uchel silicon nitrid yn well.
Cemeg catalytig
Mewn peirianneg gemegol, defnyddir scandiwm yn aml fel catalydd, tra gellir defnyddio Sc2O3 ar gyfer dadhydradu a dadocsideiddio ethanol neu isopropanol, dadelfennu asid asetig, a chynhyrchu ethylen o CO a H2. Mae'r catalydd Pt Al sy'n cynnwys Sc2O3 hefyd yn gatalydd pwysig ar gyfer prosesau puro a mireinio hydrogeniad olew trwm yn y diwydiant petrocemegol. Mewn adweithiau cracio catalytig fel Cumene, mae gweithgaredd catalydd seolit Sc-Y 1000 gwaith yn uwch na gweithgaredd catalydd silicad alwminiwm; O'i gymharu â rhai catalyddion traddodiadol, bydd rhagolygon datblygu catalyddion scandiwm yn ddisglair iawn.
Diwydiant ynni niwclear
Gall ychwanegu ychydig bach o Sc2O3 at UO2 mewn tanwydd niwclear adweithydd tymheredd uchel osgoi trawsnewid dellt, cynnydd mewn cyfaint, a chracio a achosir gan drawsnewid UO2 i U3O8.
Cell tanwydd
Yn yr un modd, bydd ychwanegu 2.5% i 25% o scandiwm at fatris nicel alcali yn cynyddu eu hoes gwasanaeth.
Bridio amaethyddol
Mewn amaethyddiaeth, gellir trin hadau fel corn, betys, pys, gwenith a blodyn yr haul â sylffad scandiwm (mae'r crynodiad fel arfer yn 10-3 ~ 10-8mol / L, bydd gan wahanol blanhigion wahanol), a chyflawnwyd yr effaith wirioneddol o hyrwyddo egino. Ar ôl 8 awr, cynyddodd pwysau sych gwreiddiau a blagur 37% a 78% yn y drefn honno o'i gymharu ag eginblanhigion, ond mae'r mecanwaith yn dal i gael ei astudio.
O sylw Nielsen i ddyled data màs atomig hyd heddiw, dim ond ers cant neu ugain mlynedd y mae scandium wedi dod i olwg pobl, ond mae bron wedi eistedd ar y fainc am ganrif. Dim ond datblygiad egnïol gwyddoniaeth ddeunyddiau ddiwedd y ganrif ddiwethaf y daeth â bywiogrwydd iddo. Heddiw, mae elfennau daear prin, gan gynnwys scandium, wedi dod yn sêr poeth mewn gwyddor deunyddiau, gan chwarae rolau sy'n newid yn barhaus mewn miloedd o systemau, gan ddod â mwy o gyfleustra i'n bywydau bob dydd, a chreu gwerth economaidd sydd hyd yn oed yn anoddach ei fesur.
Amser postio: Mehefin-29-2023